如何让基因编辑工具既精准又安全,还能真正走进临床?第三附属医院教授王晓刚团队用最新成果给出了答案。
该团队近期发表系列研究成果,首次将蛋白-核酸约束语言模型引入碱基编辑工具设计,成功开发出结构更紧凑、编辑更精准、脱靶风险更低的新型腺嘌呤碱基编辑器(ABE),并在骨关节炎动物模型中验证了其治疗潜力。这标志着AI赋能的碱基编辑技术已具备从基础研究向临床疗法转化的能力。
碱基编辑技术能够在不造成DNA双链断裂的前提下实现单碱基精准替换,在遗传性疾病治疗、细胞治疗等领域前景广阔。其中,ABE可高效实现A•T到G•C的单碱基转换,但长期存在三大瓶颈:活性窗口宽、旁观者编辑严重以及脱靶风险高。传统蛋白质语言模型仅能提取蛋白质自身的序列特征,无法“感知”其作用底物(核酸)的特性,这一局限长期制约着基因编辑酶的精准设计。
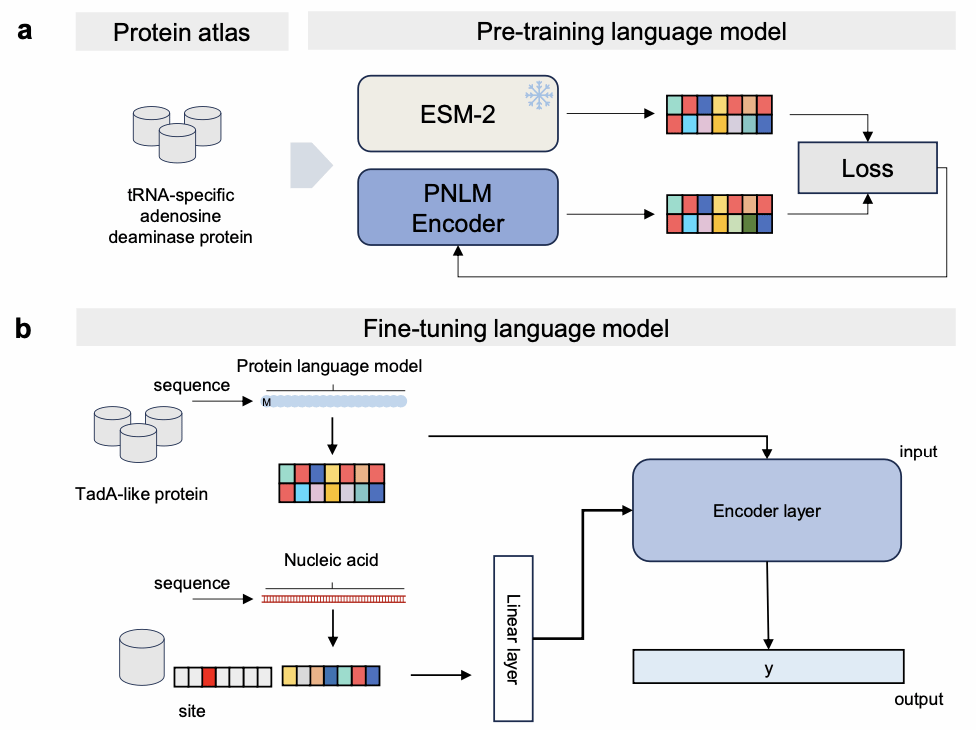
为解决上述问题,第三附属医院王晓刚团队联合苏州系统医学研究所张晓辉团队、新加坡国立大学张阳团队,在Nature Communications杂志发表了题为“Protein-Nucleic Acid Language Model-assisted Design of Precise and Compact Adenine Base Editor”的研究论文。他们首次提出蛋白-核酸约束语言模型的概念,将核酸底物序列及其编辑位点信息编码后引入蛋白质语言模型作为条件约束,使模型能够真正“理解”编辑酶与DNA底物之间的特异性相互作用关系。这使得模型在序列生成过程中自动规避可能导致编辑效率低下或脱靶效应的突变组合,从而克服了传统理性设计中突变组合筛选盲目性大、成功率低的痛点。
基于这一模型,团队生成了150个ABE8e碱基编辑器的变体序列,经过多轮严格的计算筛选和细胞功能实验验证,最终获得了结构最紧凑、编辑性能最优的变体——PNLM-pcABE。该变体不仅保留了高效的腺嘌呤碱基编辑能力,还显著提高了编辑精度,缩小了分子体积,为其在体内基因治疗中的递送应用提供了优势。
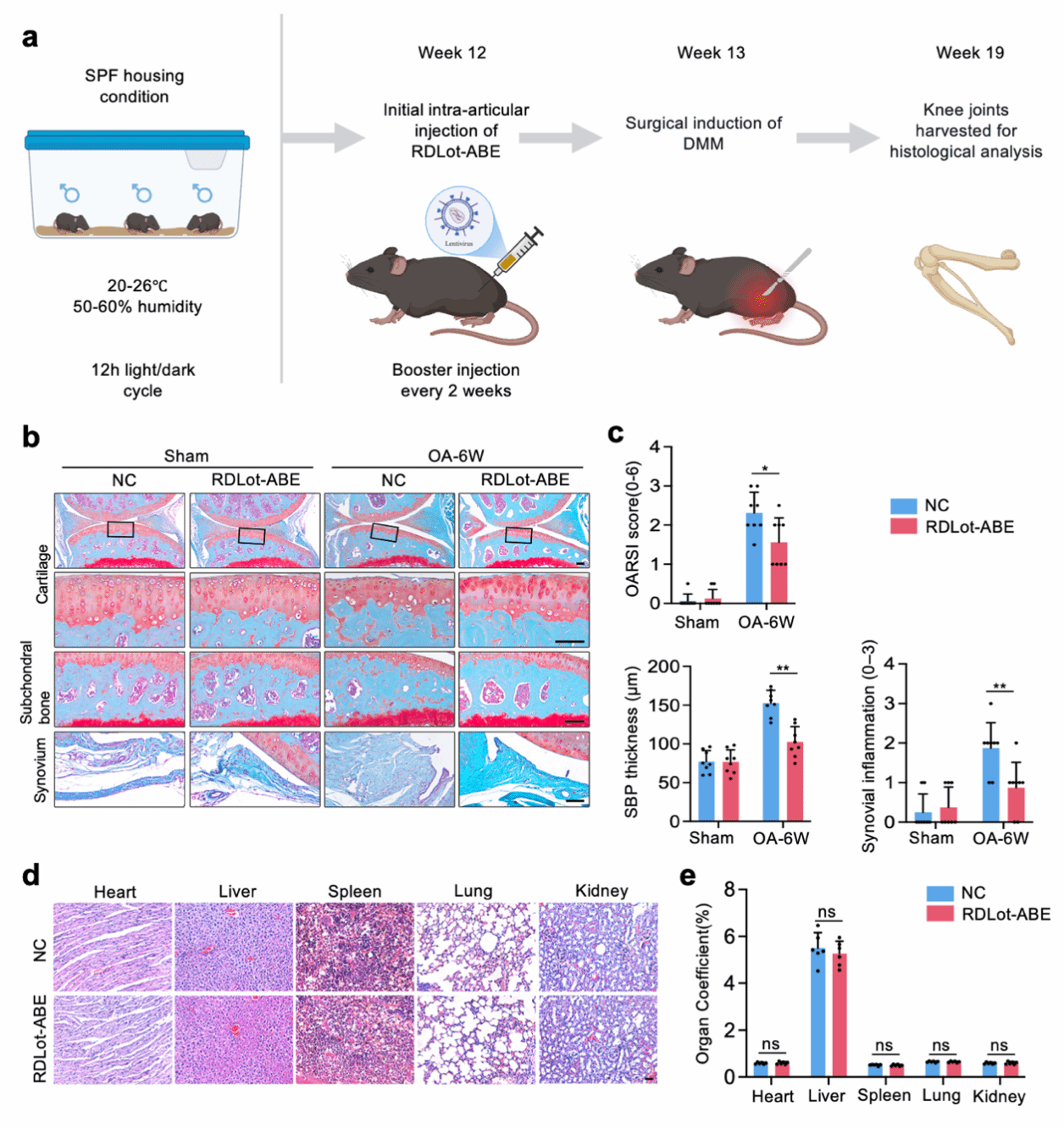
在随后的研究中,第三附属医院王晓刚团队、李凯团队和苏州系统医学研究所张晓辉团队合作在Advanced Science杂志发表了题为“Protein Large Language Model–Optimized ABE Enables Efficient and Safe Osteoarthritis Treatment”研究论文。他们通过结构嵌入的蛋白质大语言模型精准建模,筛选出新一代ABE8e变体RDLoT-ABE。联合团队发现,RDLoT-ABE不仅保留了ABE8e的编辑活性,而且编辑精度进一步提升,脱靶效率显著降低,为临床治疗提供了安全性保障。
在临床应用层面,团队通过关节腔递送的方式,使用RDLoT-ABE精准靶向骨关节炎中软骨退化的关键基因FSCN1。结果显示,该工具在小鼠骨关节炎模型中展现出良好的软骨保护作用与优异的生物安全性。这种保护效果在人源软骨外植体中也得到验证,为其临床转化提供了关键证据。这一成果不仅为骨关节炎疾病提供了全新治疗方案,也展示了AI设计的高精度碱基编辑器从实验室走向临床的巨大潜力。
目前,团队累计获批3项国家发明专利、3项软件著作权。据悉,相关研究成果转化也正在洽谈中。