近日,药学院周平正教授、刘叔文教授团队联合香港教育大学翁建霖教授团队破解肠道稳态调控密码,揭示了体积调控型阴离子通道VRAC在维持肠上皮细胞功能平衡中的关键作用,为炎症性肠病的发病机制及潜在治疗策略提供了新的理论依据。
VRAC(Volume-regulated anion channel)被认为是最重要的渗透压敏感离子通道,响应渗透压变化激活,通过介导氯离子及多种有机阴离子跨膜转运,在细胞体积调节、代谢稳态及免疫反应中发挥关键作用。肠上皮屏障是人体最大的内屏障,时刻面临水和食物带来的动态渗透压变化,然而渗透压变化如何通过VRAC调控肠上皮屏障仍是未知领域。研究团队应用肠上皮特异性VRAC缺陷小鼠、结合炎症性肠病模型,探究VRAC在肠上皮屏障系统中的调控作用。
研究发现,在正常情况下VRAC缺失对肠上皮结构影响有限,但在炎症条件下,VRAC缺陷小鼠出现更严重的肠道损伤和炎症反应,并促进炎症相关结直肠癌的进展。进一步分析显示,VRAC缺失不影响干细胞的数量和谱系分化倾向,而是特异性地改变吸收型肠上皮细胞沿隐窝-肠腔轴的空间分布,使承担营养吸收功能的成熟细胞减少,而与抗菌防御相关的细胞比例增加,从而打破肠上皮细胞在代谢与防御两种功能之间的平衡。
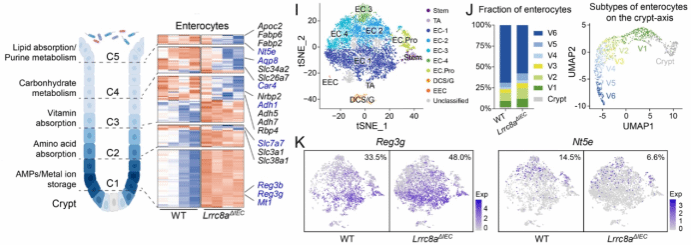
肠上皮细胞特异性VRAC缺失改变吸收型肠上皮细胞沿隐窝-肠腔轴的空间分布
机制研究表明,VRAC缺失通过抑制BMP信号通路,干扰吸收型肠上皮细胞的分化。在VRAC缺失的肠上皮细胞中,视黄酸代谢受影响最为显著,而补充视黄酸可逆转其所致的炎症反应加剧。另一方面,VRAC缺失促进抗菌肽产生型肠上皮细胞比例增加,从而扰乱肠道菌群稳态;给予乳杆菌属(Lactobacillus)干预可有效恢复菌群平衡并缓解炎症。
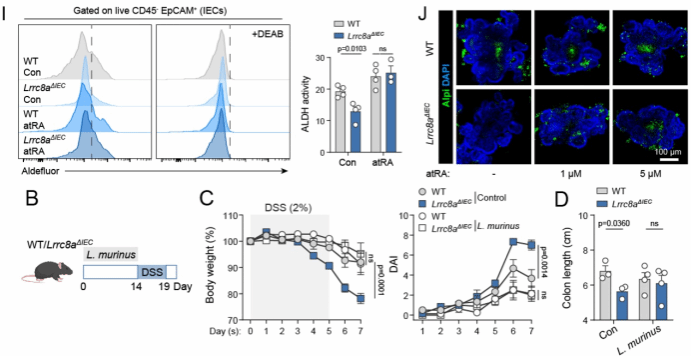
补充视黄酸或乳酸杆菌可逆转VRAC缺失引起的肠道损伤
综上,该研究揭示了VRAC在肠上皮细胞中的关键调控作用:VRAC通过调控吸收型肠上皮细胞沿隐窝-肠腔轴的空间分布,在营养吸收与抗菌防御之间建立动态平衡,维持肠道稳态,为炎症性肠病的防治提供了新的潜在靶点。
研究成果在Nature Communications发表,题为“VRAC coordinates the trade-off between nutrient absorption and antimicrobial defense in enterocytes against inflammation”,药学院博士后易欣、暨南大学副研究员张世卿、药学院博士生顾心培、吴晓燕为本文共同第一作者,周平正教授、翁建霖教授和刘叔文教授为共同通讯作者。
