结直肠癌(Colorectal cancer,CRC)作为全球第三大常见恶性肿瘤,其发病率与死亡率逐年攀升。越来越多的研究表明,肠道菌群失调可通过代谢产物异常参与CRC的发生发展,但关键效应分子及其作用机制仍有待阐明。细菌细胞壁降解并释放的肽聚糖片段在维持肠道稳态中发挥重要作用,但其在CRC中的具体作用尚未明确。
近日,珠江医院何肖龙、周宏伟、崔春晖团队与广州医科大学附属第二医院高杰团队合作,揭示了肠道菌群来源的N-乙酰胞壁酸通过靶向AKT1信号通路抑制结直肠癌进展的分子机制,为CRC防治提供了新策略。
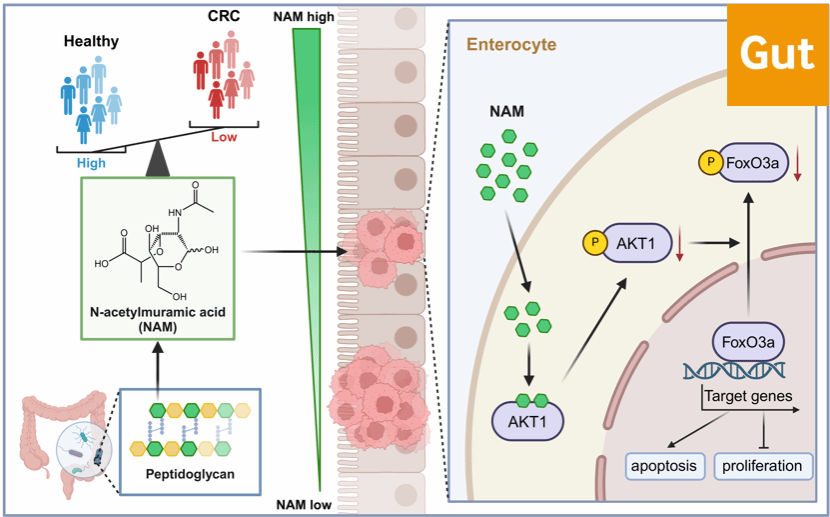
研究团队通过对7个跨国CRC队列的宏基因组数据分析,发现CRC患者肠道菌群中肽聚糖合成酶的基因丰度显著降低,再通过靶向代谢组学检测发现,肽聚糖片段N-乙酰胞壁酸(NAM)在CRC患者的粪便及血清样本中均显著降低,进一步提示菌群代谢紊乱导致的NAM缺失可能与CRC发生存在潜在关联。
为验证NAM的生物学功能,研究团队通过构建多种CRC小鼠模型及CRC患者来源的类器官模型,发现补充NAM可显著延缓小鼠CRC进展并抑制肿瘤类器官生长。在机制研究中,通过20K人类蛋白质芯片筛选结合蛋白分子互作实验,首次证实NAM可直接结合AKT1蛋白。该互作能够抑制AKT1 Ser473和Thr308位点的磷酸化,进而阻断AKT1-FoxO3a信号通路的活化,最终通过抑制肿瘤细胞增殖并促进其凋亡来抑制CRC进展。
本研究首次揭示了肠道菌群代谢物NAM通过靶向AKT1-FoxO3a信号通路抑制CRC进展的分子机制。这一发现不仅为CRC的发生机制提供了新的见解,也为开发针对菌群代谢产物的精准治疗策略提供了重要的理论依据。
该研究在胃肠病学顶级期刊《Gut》发表,论文题为“Gut microbial-derived N-acetylmuramic acid alleviates colorectal cancer via the AKT1 pathway”,珠江医院何肖龙、周宏伟、崔春晖和广州医科大学附属第二医院高杰为论文共同通讯作者,珠江医院博士后胡梦瑶和博士研究生徐轶、王宇清和黄祯荷为论文共同第一作者。