骨关节炎治疗取得新进展
骨关节炎作为全球最常见的关节疾病,如同“关节软骨的无声侵蚀者”,导致患者疼痛、僵硬甚至残疾。现有止痛药和抗炎治疗仅能暂时缓解症状,却无法阻止软骨持续退化。深圳医院研究团队近年发现,关节内过度活跃的Wnt/β-catenin信号通路就像“失控的生长开关”,加速软骨破坏。虽然β-catenin小分子抑制剂MSAB能有效抑制该通路,但如何精准作用于关节软骨,降低药物副作用,始终是治疗突破的瓶颈。
近日,深圳医院教授陆克研究团队与中国科学院深圳先进技术研究院教授陈棣和潘宏科研团队在《Bioactive Materials》发表突破性成果,文章不仅解析了MSAB抑制关节炎的β-catenin/DDR2致病通路的新机制,同时开发了人血清白蛋白“纳米快递车”这一新的关节炎给药体系,成功实现关节精准投送。动物实验显示,该疗法使软骨损伤减少70%,同时显著缓解疼痛。
本研究通过体内体外实验,验证了该给药体系能够有效靶向软骨细胞,减轻软骨退化,为骨关节炎疾病的分子机制提供了新的见解,为骨关节炎的治疗提供了新的策略。
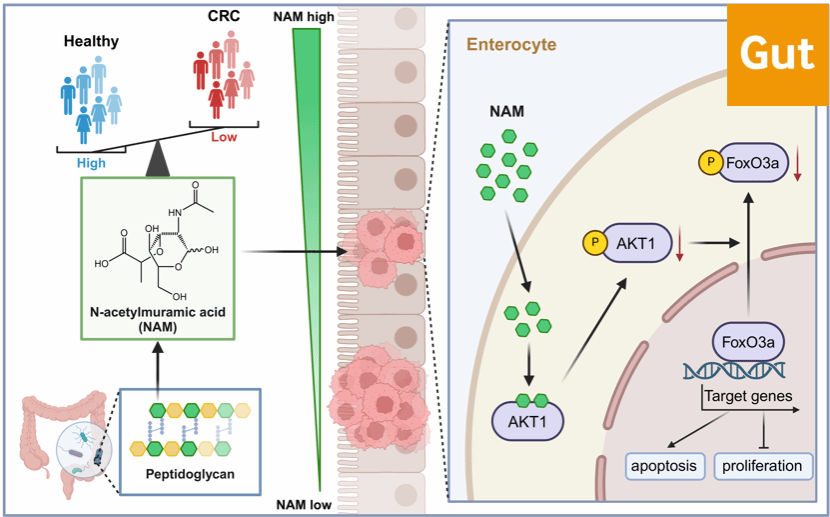
治疗骨关节炎的“智能纳米颗粒”
研发出“智能骨修复支架”(PMns)
难治性骨缺损是骨科治疗中常见的顽固难题,尤其是长期使用激素引发的骨坏死(SAON)患者,常面临着新骨生长缓慢、血管再生困难的双重困境。这类损伤不仅自身修复能力差,还会引发过度的炎症反应,形成阻碍愈合的恶性循环。现有疗法往往难以同时解决骨骼再生、血管重建和免疫调节三大关卡,因此导致治疗效果受限。
近日,深圳医院桑宏勋团队与中国科学院深圳先进技术研究院赖毓霄团队合作采用3D打印技术,研发出一种“智能骨修复支架”(PMns)。这种由可降解材料与二氧化锰纳米颗粒组成的支架,这种支架能够主动清除损伤部位的有害物质(活性氧ROS),同时通过调节免疫细胞状态(将促炎的M1型巨噬细胞转化为修复型的M2型),为骨再生创造了有利环境。
实验显示,该支架不仅能显著提升干细胞成骨能力,促进钙盐沉积,还能同步刺激血管新生。这种“骨修复-血管重建”同时展开的创新设计,在动物实验中得到了有效验证,为激素性骨坏死等顽固性骨缺损带来了新的治疗策略,相关成果已发表于学术期刊《Bioactive Materials》。
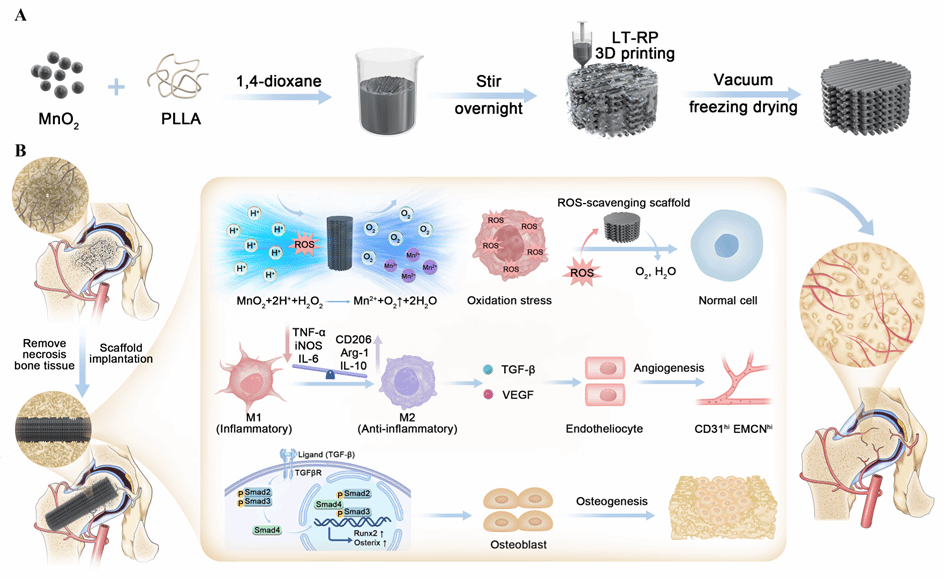
治疗激素性骨坏死 “智能骨修复支架”
创新性利用PDSC细胞微球类器官自组装形成“活体骨膜”
骨缺损修复领域长期面临“供体不足、再生失衡”的困境,骨膜作为覆盖在骨骼表面的关键组织,富含干细胞与血管网络,因此人工骨膜常被用于治疗和研究该疾病。但传统人工骨膜多停留在模仿纤维结构的初级阶段,难以还原其促进血管新生与骨骼再生的双重功能。有研究发现,骨膜来源干细胞(PDSCs)具有更强的抗衰老和成骨能力,但如何将其转化为可临床应用的仿生骨膜,始终是未被解决的难题。
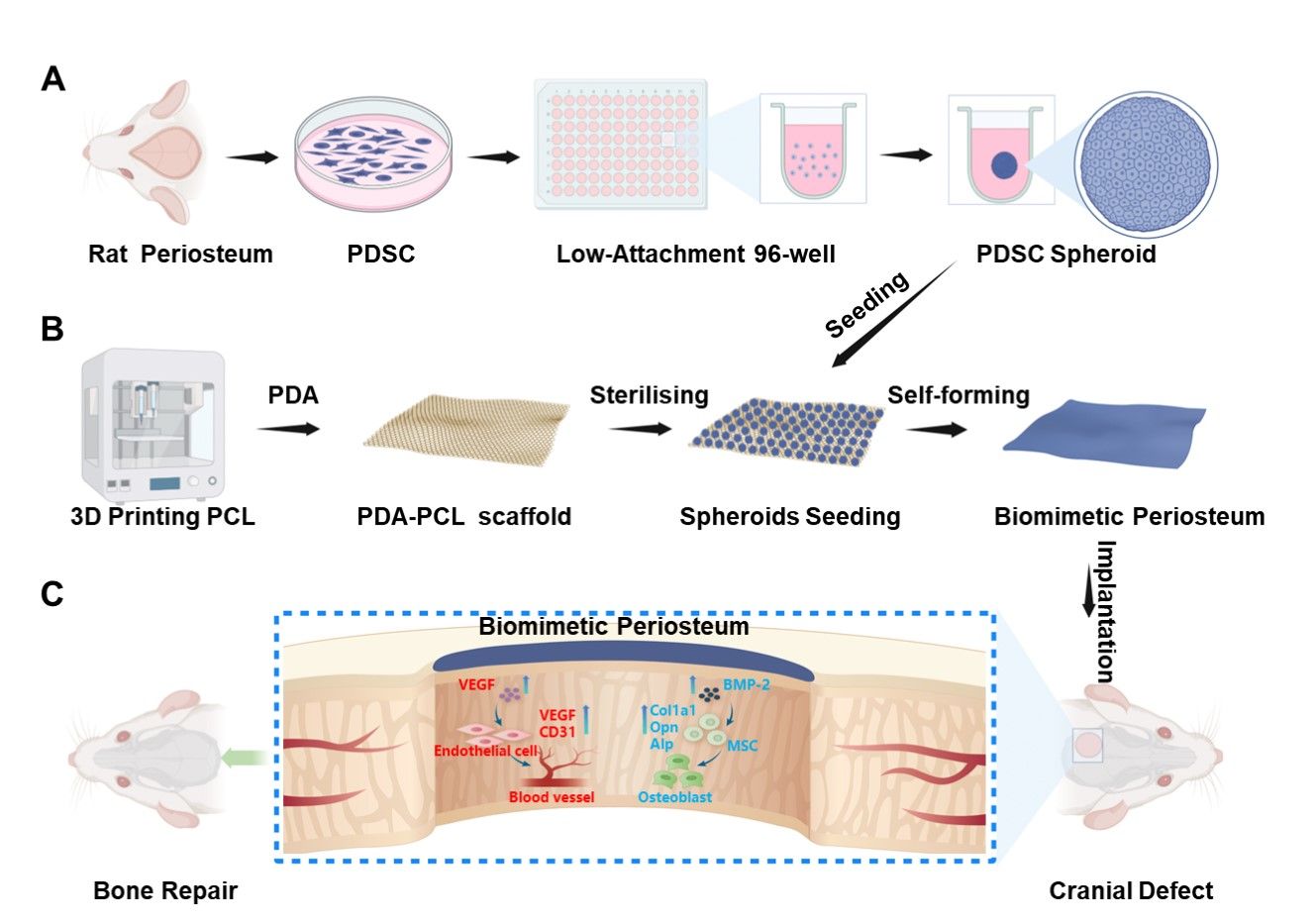
治疗大段骨缺损的“智能活性骨膜”
深圳医院桑宏勋团队在《Acta Biomaterialia》发表重要成果,创新性利用PDSC细胞微球类器官自组装形成“活体骨膜”。研究人员通过3D打印技术构建可降解支架,结合聚多巴胺涂层提升材料活性,再将PDSCs培育成精密的三维球状体(细胞微球类器官)。这些直径约150微米的细胞微球可持续释放BMP2和VEGF两大关键因子,同时驱动骨骼再生与血管新生。动物实验显示,新型骨膜使缺损区域血管密度提升3倍,8周内骨再生量超过传统方法的2倍。这种能自主调控微环境的智能骨膜,使得骨修复治疗不仅兼顾了“结构替代”的传统方法,更加注重了“功能重建”的新方法,为骨缺损修复领域提供了新的治疗策略。
