近日,基础医学院熊符团队在口腔科学领域国际权威期刊Int J Oral Sci杂志(一区)上,发表了题为“Double heterozygous pathogenic mutations in KIF3C and ZNF513 cause hereditary gingival fibromatosis”的研究论文。
遗传性牙龈纤维瘤病(hereditary gingival fibromatosis,HGF;OMIM:135300)是一种牙龈组织纤维化瘤样增生的遗传性疾病,目前只能通过手术进行阶段性治疗,而手术后易复发,给HGF患者及其家庭带来沉重的心理和经济负担,对HGF的致病基因寻找及发病机制研究是预防、诊治该病的基础。该病分为5型,目前针对2型和3型的致病基因都还没报道。在本研究中研究者收集一个到包含9名HGF患者的26人次大家系,通过外显子测序、生物信息分析、家系内共分离和单倍型分析克隆到了致病新基因ZNF513(c.C748T,p.R250W)和KIF3C(c.G1229A,p.R410H)的双杂合致病突变,该两个致病基因都位于2p23.3上,属于HGF 3型。研究发现基因突变后导致牙龈原代成纤维细胞中相应蛋白表达增高,细胞增殖和迁移能力明显增强;基因敲入小鼠模型进一步证实,单纯Zfp513(p.R250W)或Kif3c(p.R412H)的杂合或纯合突变不会导致明显的牙龈增生表型,而双基因突变会导致牙龈一定程度增生。研究证实在牙龈成纤维细胞中转录因子ZNF513与KIF3C exon1结合互作并参与KIF3C表达的正向调节;研究还发现ZNF513与HGF重要致病基因SOS1启动子结合,在SOS1的表达调控中起着重要的调控作用。此外,KIF3C p.R410H突变可激活与细胞纤维化密切相关的PI3K和KCNQ1钾通道。最后研究证实,ZNF513联合KIF3C可通过PI3K/AKT/mTOR和Ras/Raf/MEK/ERK通路共同调控牙龈成纤维细胞的增殖、迁移和纤维化反应。该研究发现报道了HGF 3型致病新基因和发病机制,为该类疾病的临床分子诊断、药物开发、遗传咨询及辅助生殖提供了实验和理论依据。
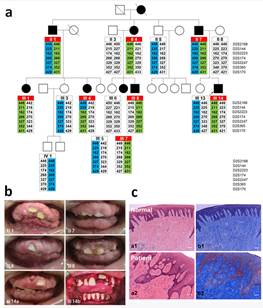

Pedigree-based mapping and mechanism on HGF-causing mutations in in KIF3C and ZNF513
杂志社编辑部认为该论文的研究成果为相关领域做出了重大贡献,决定由编辑部赞助文章的处理费,不收取任何版面费用(信件原文:Your paper is considered to be a significant contribution to the field, and we appreciate the opportunity to publish it in this journal. We are pleased to inform you that your article-processing charge (APC) will sponsored by Editorial Office)。
南方医科大学基础医学院陈见凡博士和深圳六院精准医学中心许雪青主任为本文并列第一作者,熊符教授和南方医院张磊涛副主任医师为共同通讯作者。